2021年12月15日,来自纽约哥伦比亚大学医学院的汪丽恒和Domenico Accili在Cell Metabolism杂志上发表文章TOX4, an insulin receptor-independent regulator of hepatic glucose production, is activated in diabetic liver,鉴定出TOX4作为一个激素效应型转录因子调控肝脏Pck1的转录。抑制肝细胞的TOX4减少糖异生,提高糖耐量。在高脂饮食诱导的肥胖小鼠和糖尿病小鼠中,降低肝脏TOX4表达可缓解高血糖症。TOX4与FoxO1对于HGP过程的调控具有累加效应,且TOX4的调控作用不依赖于胰岛素受体。

研究人员利用biotin标记激素响应基因Pck1启动子序列作为诱饵,在原代肝细胞中进行DNA pull-down实验,利用质谱鉴定调控Pck1的转录因子。发现地塞米松和cAMP(D/C)诱导后,TOX4被招募到Pck1启动子区域,胰岛素的添加则会降低这种结合,而FoxO1和CREB1有类似的现象。D/C处理增加TOX4蛋白水平,但不影响细胞核中TOX4水平。荧光素酶报告基因检测显示,TOX4可调控糖异生相关基因G6pcp和Pck1p的转录。随后,研究人员在细胞水平和小鼠水平证明,肝细胞中Tox4敲低或敲除导致葡萄糖产生减少,糖异生相关基因表达减少,葡萄糖耐受改善。此外,TOX4调控肝脏葡萄糖代谢不依赖于胰岛素受体信号。
TOX4对于糖异生的调控作用类似于FoxO1,两者之间的作用关系如何?研究人员构建了TOX4/FoxO1双敲除(DKO)小鼠,相比于单敲除小鼠,DKO在葡萄糖耐受、丙酮酸耐受、对PCK1的mRNA和蛋白的调控,以及G6pc和Ppargc1a基因表达的调控中都表现出累加效应。进一步研究显示,TOX4与Pck1的-117至-68 bp和-51至-1 bp之间的顺式作用元件结合,不同于FoxO1的顺式作用元件,但FoxO1的结合缺失会削弱TOX4的调控作用。此外,FoxO1和TOX4的互作不依赖于cAMP处理,但会被胰岛素抑制;cAMP处理会诱导TOX4和CREB互作,胰岛素处理会抑制两者互作。Pck1p基因的TOX4的结合位点与CREB反应元件具有重叠,两者对于其转录调控具有累加效应。敲除CRE序列则完全消除TOX4和/或CREB对Pck1p的转录调控,说明TOX4调控HGP,部分是通过与CREB互作来实现的。
HGP增加可导致T2D病人的空腹高血糖,那么TOX4是否参与这个过程?相比健康对照,糖尿病NAFLD病人的肝活检样本中TOX4水平增加10倍,G6PC水平增加,意味着糖异生增加。而且,HFD诱导的肥胖小鼠中也观察到TOX4的增加。随后,研究人员利用shRNA降低肝脏Tox4的表达,则可以有效降低肥胖小鼠的血糖和提高葡萄糖耐受来改善其葡萄糖代谢。利用T2D db/db遗传小鼠模型,同样观察到TOX4表达增加,降低其表达可缓解小鼠的高血糖症和葡萄糖不耐受。
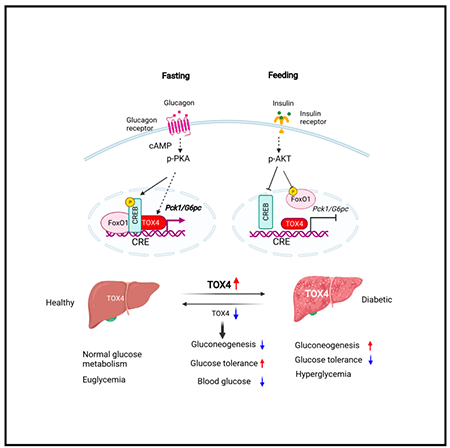
总的来说,文章发现TOX4参与激素调控肝脏葡萄糖产生过程,且不同于胰岛素-FoxO1调控通路。糖尿病人或模型小鼠的肝脏中TOX4表达增加,抑制TOX4可降低高血糖,改善糖耐量,提示TOX4参与糖尿病的病理发生,或为研究糖尿病的病理和治疗提供新的视角。

原文链接:
https://doi.org/10.1016/j.cmet.2021.11.013













